07 JUILLET 2025
Analyse des risques d’usage : comment l’aborder selon la norme EN 62366-1 ?
Aptitude à l'utilisation

Lorsqu’on parle d’analyse des risques pour un dispositif médical, on pense souvent à l’ISO 14971. Mais dès qu’on s’intéresse à l’interaction entre l’utilisateur et le dispositif, c’est la norme EN 62366-1:2015/A1 :2020 qui prend le relais.
Et c’est là que beaucoup de fabricants s’interrogent :
• Comment identifier les erreurs d’utilisation potentielles ?
• Faut-il les intégrer dans l’analyse globale des risques ?
• Et surtout, comment structurer une vraie analyse des risques d’usage ?
A travers cet article, nous allons répondre à ces questions.
Pourquoi réaliser une analyse des risques d’usage ?
Parce qu’un dispositif peut être techniquement sûr, mais dangereux en cas de mauvaise utilisation.
L’objectif de cette analyse est simple : anticiper les erreurs d’utilisation probables et adapter l’interface utilisateur (IU) pour les éviter ou en limiter les conséquences.
C’est une exigence de la norme EN 62366-1, qui impose d’identifier les scénarios d’utilisation relatifs au phénomène dangereux, autrement dit, les scénarios d’utilisation susceptibles de provoquer un danger suite à une erreur d’utilisation.
Quel lien avec la norme ISO 14971 ?
La norme EN 62366-1 ne remplace pas l’ISO 14971 : elle la complète.
Là où l’ISO 14971 définit le cadre global de gestion des risques, l’EN 62366-1 se concentre sur les risques liés à l’interaction homme-machine.
Concrètement :
• L’analyse des risques d’usage doit s’intégrer dans la documentation de gestion des risques de l'ISO 14971,
• Mais elle repose sur une méthodologie spécifique, centrée sur l’utilisateur, décrite dans l’EN 62366-1.
Quelles sont les étapes clés de l’analyse des risques d’usage selon la norme EN 62366-1 ?
La norme EN 62366-1 définit 3 étapes clés (clause 5.2 à 5.4) pour réaliser l’analyse des risques d’usage :
1. Identifier les caractéristiques de l’interface utilisateur liées à la sécurité et les erreurs d’utilisation potentiellesQuand la réaliser ?
Cela revient à se demander :
Quelles parties de l’interface utilisateur peuvent influencer la sécurité du dispositif ?
Cela inclut :
• Les éléments physiques ou logiciels manipulés par l’utilisateur (boutons, écrans, connecteurs…) ;
• Les messages d’alerte, les couleurs, les codes visuels ;
• La documentation d’accompagnement (ex : contre-indications dans la notice) ;
• Tout ce qui peut prêter à confusion, être oublié ou mal interprété.
Pour identifier ces éléments, il est possible d’utiliser la liste des questions disponibles dans l’ISO/TR 24971:2020 (A.2.31 à A.2.37).
Ensuite, en se basant sur la spécification d’utilisation et les caractéristiques de l’interface, il est nécessaire d’identifier les erreurs d’utilisations qui peuvent survenir. Cette identification peut notamment être réalisée grâce à une analyse des tâches.
2. Identifier les dangers et situations dangereuses connus ou prévisiblesCombien en réaliser ?
Cela revient à se demander :
Quels sont les dangers et situations dangereuses relatifs à l’utilisation du dispositif qui pourraient affecter le patient, l’utilisateur ou d’autres personnes ?
Lors de cette identification, il est nécessaire de prendre en compte :
• La spécification d’utilisation (clause 5.1), notamment les profils utilisateurs ;
• Les informations existantes concernant les dangers et situations dangereuses pour les dispositifs similaires ;
• Les erreurs d’utilisation identifiées lors de l’étape précédente.
3. Identifier et décrire les scénarios d’utilisation relatifs au phénomène dangereuxSur quels éléments de l’interface utilisateur ?
Cela revient à se demander :
Quels scénarios d’utilisation peuvent mener aux dangers et situations dangereuses identifiés ?
Pour chacun des scénarios identifiés, il faut documenter toutes les tâches associées, leurs séquences et la sévérité du dommage associé.
Autrement dit :
1. On identifie ce qui peut impacter l’usage au niveau de l’interface.
2. On décrit les potentiels dangers associés à l’utilisation du dispositif.
3. On décrit les scénarios qui peuvent mener à ces dangers.
Quel est l’impact de l’analyse des risques sur la conception ?
Votre analyse des risques va faire émerger des scénarios critiques. Il faudra alors identifier des mesures de maîtrise du risque pour réduire la probabilité d’apparition des erreurs et rendre les risques résiduels acceptables.
Pour se faire, vous allez donc identifier plusieurs mesures de maîtrise du risque qu’il faudra intégrer dans la conception de votre interface utilisateur.
Autrement dit, il est indispensable de prendre en compte l’analyse des risques d’usage dans la conception.
Comment structurer l’analyse des risques ?
Vous pouvez intégrer votre analyse des risques d’usage dans votre analyse des risques globale en créant notamment une balise ou un tag “usage”.
Nous vous conseillons néanmoins de réaliser une « Use Related Risk Analysis » (uRRA) pour favoriser l’identification et les échanges avec les autorités, notamment si vous prévoyez une soumission FDA.
Un exemple ?
Le tableau ci-dessous est un exemple de possibles dangers, associés à un scénario d’utilisation relatif au phénomène dangereux, le dommage associé et des potentielles mesures de maitrise du risque. L’erreur d’utilisation est quant à elle soulignée.
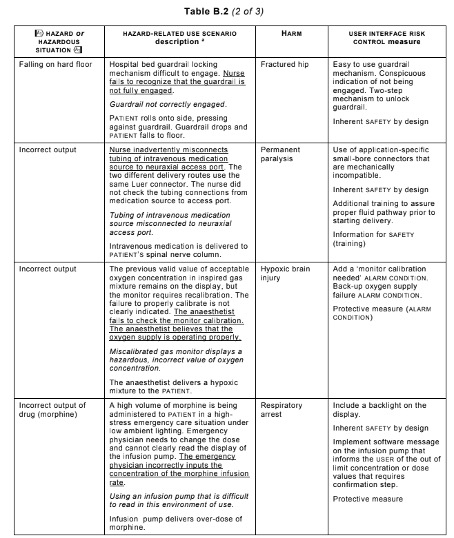
Table B.2 norme EN 62366-1 :2015/A1 :2020
En résumé
• L’analyse des risques d’usage repose sur trois étapes clés de la norme EN 62366-1 (caractéristiques IU, dangers, scénarios).
• Elle est centrée sur les erreurs d’utilisation plausibles, pas seulement les défaillances techniques.
• Elle s’articule avec la gestion des risques globale selon l’ISO 14971.
• Elle doit être documentée, traçable, et utilisée pour guider la conception.