Du marquage CE au 510(k) : retour d’expérience sur l’accompagnement usability du dispositif DBLG2 de Diabeloop


Contexte du projet
Le système DBLG2 est un dispositif médical en boucle fermée destiné à l’aide à la gestion du diabète pour les patients de type 1. Il s’inscrit dans un usage quotidien, avec des interactions fréquentes entre l’utilisateur, le dispositif et son environnement.
Dans ce contexte, la compréhension des informations affichées, la bonne réalisation des actions attendues et la prévention des erreurs d’utilisation constituent des enjeux majeurs, tant pour la sécurité des patients que pour l’efficacité du traitement.
En Europe, le dispositif est destiné à une population adulte. Dans le cadre de la démarche FDA, la revendication d’usage inclut également des utilisateurs adolescents, introduisant des enjeux spécifiques en matière de compréhension, d’autonomie et d’accompagnement lors de l’utilisation du dispositif.
Sur le plan réglementaire, le projet s’est inscrit dans deux cadres successifs :
• Le marquage CE, dans un contexte de transition vers le règlement MDR,
• Puis une soumission FDA ayant conduit à l’obtention d’un 510(k).
Les enjeux côté Diabeloop
• Quels étaient vos principaux enjeux en matière d’aptitude à l’utilisation pour le dispositif DBLG2 ?
Notre enjeu était de valider la sécurité de notre produit, son ergonomie et sa facilité d’utilisation. Au-delà de l’aspect purement réglementaire, ces tests étaient l’occasion de vérifier la satisfaction et le désir d' utilisation côté utilisateur via les debriefs, et de récolter un feedback direct très utile pour orienter nos futures évolutions.
• Qu’est ce qui rend, selon vous, un dossier usability particulièrement complexe à construire et sécuriser ?
La complexité majeure réside dans le fait de réussir à simuler des situations réelles d'utilisation, ce qui s'avère parfois très compliqué en environnement de test. Il faut pouvoir reproduire les conditions du quotidien de manière crédible pour s'assurer de la robustesse du système.
• Quelles difficultés aviez-vous identifiées en interne (interprétation des exigences, organisation des tests, articulation avec le développement, contraintes planning, etc.) ?
Nous faisions face à deux défis principaux. Tout d’abord, une forte contrainte de planning : l’étude devait être réalisée dans un temps imparti très court. Ensuite, spécifiquement pour la FDA, la rédaction des justifications concernant l’analyse des risques résiduels était un travail dont nous n’avions pas l’habitude en interne. Sur ce point, l’encadrement et l'expérience d’Usarea nous ont permis de construire un argumentaire qui répondait parfaitement aux attentes des autorités.
Approche mise en place et déroulement des travaux
Accompagnement pour le marquage CE
Dans le cadre du marquage CE, Usarea a accompagné Diabeloop dans la définition et la mise en œuvre de l’évaluation de l’aptitude à l’utilisation du système DBLG2.
L’accompagnement a porté sur :
• La rédaction du protocole d’évaluation, en cohérence avec la norme EN 62366-1 et les spécificités du dispositif,
• La réalisation des tests utilisateurs, menés en région grenobloise auprès de patients adultes et de professionnels de santé,
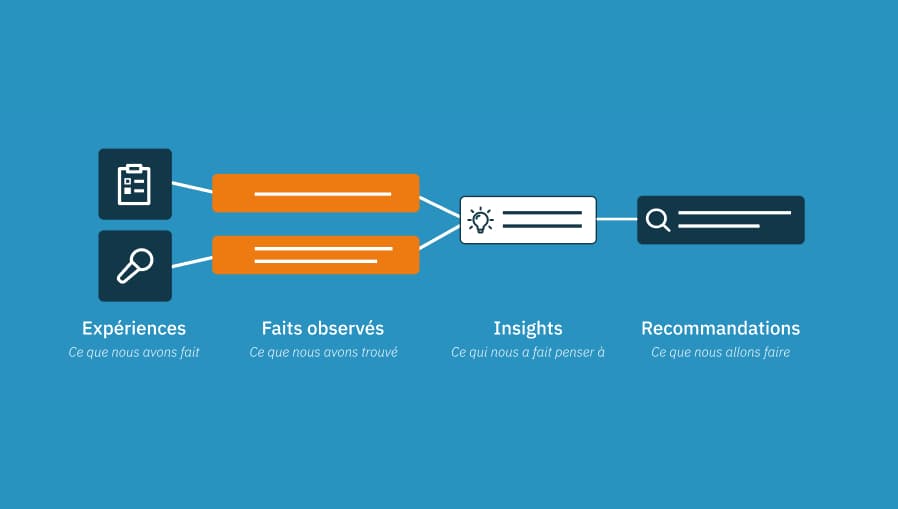
• L’analyse des résultats issus des observations et des retours utilisateurs,
• La rédaction du rapport de résultat et de la synthèse du dossier d’aptitude à l’utilisation destiné au dossier réglementaire.
Les travaux ont été menés en étroite collaboration avec les équipes Diabeloop, afin d’assurer une bonne compréhension des enjeux produit, des choix de conception existants et des contraintes de développement. Les équipes Diabeloop ont également participé aux tests utilisateurs, après avoir été formées aux bonnes pratiques de conduite des sessions et aux points de vigilance associés.
Accompagnement pour la FDA (510(k))
Dans un second temps, Usarea a accompagné Diabeloop dans la préparation et la réalisation des activités d’aptitude à l’utilisation nécessaires à la soumission FDA.
Cette phase a notamment inclus :
• La relecture et l’adaptation du protocole d’évaluation afin de répondre aux attentes spécifiques de la FDA,
• L’organisation du recrutement des utilisateurs aux États-Unis,
• La soumission à un IRB ,
• La réalisation des tests utilisateurs sur site, avec une organisation en trinôme associant pour chaque test, une personne d’Usarea et deux personnes de Diabeloop,
• L’analyse des résultats et la rédaction du rapport,
• Le support lors de l’évaluation des risques résiduels d’utilisation,
• Et la mise à jour du Human Factors Engineering Report.
Dans le cadre des revendications FDA, les tests ont intégré des modalités spécifiques :
• Des tests en dyade pour les utilisateurs adolescents, réalisés avec un accompagnant,
• Ainsi que des tests en dyade pour certains utilisateurs adultes nécessitant une assistance dans l’utilisation du dispositif.
Ces modalités ont permis de reproduire fidèlement les conditions réelles d’utilisation et d’intégrer les interactions entre l’utilisateur principal et la personne apportant un soutien lors de l’usage du dispositif.
Points clés de la collaboration
Plusieurs éléments ont structuré la démarche d’accompagnement tout au long du projet :
• Une collaboration étroite et continue: les équipes Usarea et Diabeloop ont travaillé en interaction régulière, tant en phase de préparation que lors des tests utilisateurs et de l’analyse des résultats.
• Une capacité d’adaptation face aux imprévus : le projet a nécessité des ajustements liés à des contraintes de terrain, notamment en lien avec les formations, la disponibilité des utilisateurs et les évolutions de planning. Ces éléments ont été intégrés de manière pragmatique dans l’organisation des travaux.
• La prise en compte de profils utilisateurs variés et de modalités d’usage spécifiques : la démarche a intégré des modalités de test différenciées selon les marchés, notamment la réalisation de tests en dyade dans le cadre des revendications FDA.
• Une continuité méthodologique entre les marchés CE et FDA : le protocole CE mis en œuvre a servi de base méthodologique pour la préparation du dossier FDA. Celui-ci a été adapté conjointement par les équipes Diabeloop et Usarea afin de répondre aux exigences spécifiques du marché américain et aux différences de contextes d’usage.
Retour d’expérience Diabeloop
• Quel a été, selon vous, l’intérêt d’avoir le même prestataire pour l’accompagnement CE puis FDA ?
L'intérêt majeur a été de capitaliser sur leur connaissance du produit déjà acquise. Cela a permis d’instaurer un véritable climat de confiance et d’aboutir à une grande simplification de nos échanges au quotidien.
• Qu’avez-vous particulièrement apprécié dans la manière de travailler ensemble ?
Nous avons été très satisfaits de leur réactivité et de leur adaptabilité face aux inévitables imprévus d’un tel projet. Nous avons également beaucoup apprécié la pertinence de leurs conseils et de leurs réponses tout au long de notre collaboration.
• En quoi cet accompagnement vous a-t-il aidé dans la gestion du projet et dans la sécurisation de votre dossier ?
L’accompagnement nous a fait gagner en efficacité et en rapidité pour traiter le dossier. En interne, cela s’est traduit par un support fiable : nous savions que nous avions une aide solide en cas de difficulté, ce qui nous a permis d’avancer plus sereinement.
Enseignements clés
Ce projet illustre le fait qu’il n’existe pas de démarche d’aptitude à l’utilisation standardisable applicable telle quelle à tous les dispositifs, à tous les utilisateurs et à tous les marchés, mais qu’une adaptation fine est nécessaire à chaque contexte.
La mise en œuvre d’une évaluation d’aptitude à l’utilisation efficace repose sur :
• Une compréhension fine du dispositif et de ses usages,
• Une adaptation aux contextes réglementaires et culturels,
• Une collaboration étroite entre le fabricant et les équipes en charge de l’aptitude à l’utilisation,
• Et une capacité à ajuster la méthode en fonction des contraintes terrain et des profils utilisateurs.
L’accompagnement du système DBLG2, du marquage CE jusqu’à l’obtention du 510(k), s’inscrit ainsi dans une démarche globale visant à sécuriser l’utilisation du dispositif, tout en tenant compte des réalités industrielles, réglementaires et humaines propres à chaque projet.

Amandine Broussier
Spécialiste aptitude à l'utilisation chez Usarea