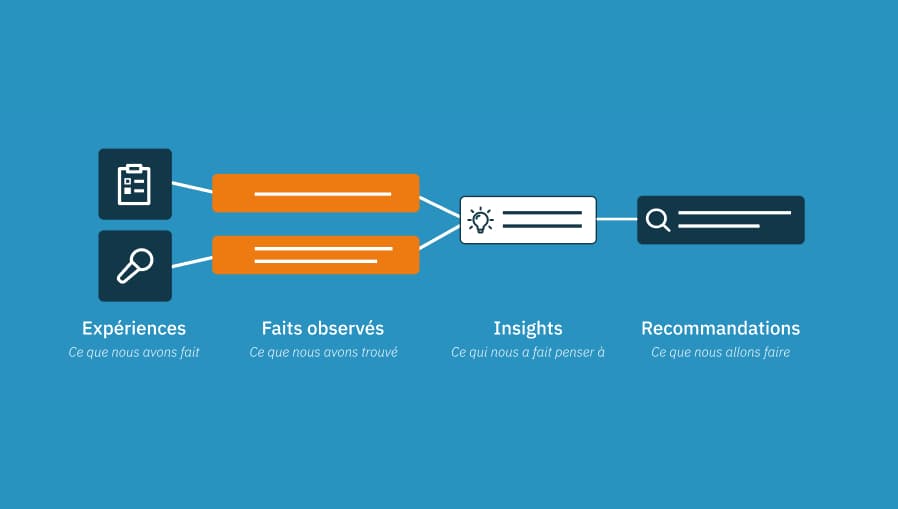
Aptitude à l’utilisation et maîtrise des risques : comment un fabricant d’instrument dentaire motorisé a sécurisé son dossier CE/FDA grâce à une approche intégrée

Contexte du projet
Une start-up, fabricant des instruments dentaires, développe un dispositif actif destiné à la manipulation de restaurations prothétiques, comme les inlays, onlays, couronnes ou facettes.
L’appareil repose sur un système de micro-pinces motorisées, dont l’ouverture et la force de préhension sont contrôlées électroniquement.
L’objectif est de permettre aux praticiens de saisir et positionner les restaurations avec une précision stable, tout en limitant les risques de chute, d’écrasement du matériau ou de mauvaise orientation dans un espace buccal réduit.
Dès les premières phases, plusieurs enjeux apparaissent :
• Structurer les activités de design control et formaliser les exigences utilisateurs ;
• Construire un processus de maîtrise des risques conforme à l’ISO 14971 ;
• Intégrer l’aptitude à l’utilisation dès le début (EN 62366-1 / FDA HFE) pour anticiper les erreurs d’usage ;
• Préparer une stratégie CE/FDA cohérente et durable.
Problématique initiale
Avant le lancement du développement formel, le fabricant avait une vision claire de ce que l’instrument devait accomplir, mais aucune structure documentaire permettant de l’industrialiser.
Les difficultés majeures étaient les suivantes :
• Exigences utilisateurs non formalisées, donc non traçables ;
• Absence de lien entre caractéristiques techniques, sécurité électrique, ergonomie et usage réel ;
• Risques d’usage non analysés (pression trop forte sur la restauration,
• Déverrouillage involontaire, mauvaise installation des embouts stériles) ;
• Aucune stratégie pour organiser l’évaluation formative puis la future évaluation sommative ;
• Classification CE et chemin FDA à clarifier.
En résumé, la start-up avançait vite sur le prototype, mais sans garanties documentaires suffisantes pour un dossier CE ou FDA.
Intervention conjointe (CSDmed + Usarea)
L’accompagnement a été structuré autour de trois flux continus : design control, maîtrise des risques et aptitude à l’utilisation.
Structuration du design control
• Mise en place d’un plan de développement définissant phases, jalons, responsabilités et livrables.
• Construction des User Requirements (URS) et Design Input Requirements (DIR) :
◦ exigences sur la force de préhension, la précision du moteur, l’endurance mécanique ;
◦ contraintes ergonomiques (poids, dimensions, prise en main) ;
◦ exigences de sécurité (IEC 60601-1 et 60601-1-6, ISO 10993, gestion des pièces réutilisables et stérilisables).
• Préparation de la traçabilité complète DIR → sorties de conception → V&V.
Maîtrise des risques
• Création du plan de gestion des risques et définition des responsabilités.
• Analyses combinant risques produit (mécaniques, électriques, logiciels si applicables) et risques d’usage.
• Travail spécifique sur les situations dangereuses liées :
◦ à la force de préhension trop élevée ;
◦ au lâcher involontaire en zone clinique ;
◦ à l’usure des embouts ou mauvais encliquetage ;
◦ à la confusion entre modes moteur.
• Ajustement du design lorsque nécessaire : limitation électronique de la force, design de sécurisation des embouts, signaux clairs indiquant l’état de la pince.
Processus usability (EN 62366-1 / FDA Human Factors)
• Définition de la spécification d’utilisation : utilisateurs, niveaux d’expérience, environnement clinique, contraintes de visibilité et d’espace.
• Identification des caractéristiques de l’interface utilisateur (UI) pouvant générer des erreurs : commandes proches, retours visuels, ressenti du moteur, force réellement appliquée.
• Élaboration de l'analyse des risques d'usage (uRRA) et des scénarios d'utilisation relatifs au phénomène dangereux.
• Sélection des scénarios critiques pour la future évaluation sommative, notamment :
◦ réglage initial de la pince ;
◦ changement d’embout en cours d’acte ;
◦ préhension et rotation simultanée de la restauration ;
◦ relâchement contrôlé en position finale.
• Réalisation d’une évaluation formative en cabinet dentaire simulé :
◦ observation des difficultés non anticipées ;
◦ adaptation de l’interface utilisateur ;
◦ simplification des gestes les plus sensibles ;
◦ documentation des améliorations dans l’UEF.
Alignement CE/FDA
• Clarification de la classification MDR et du régime CE applicable.
• Définition d’un chemin FDA basé sur la nature électronique de l’instrument et l’existence de prédicats.
• Construction d’une stratégie de V&V : tests de performance mécanique, endurance moteur, essais de préhension, conformité électrique, biocompatibilité, IP, vieillissement accéléré, tests transport.
• Préparation d’un package documentaire intégrant design control, risk management et usability sans incohérences.
Résultats obtenus
• Le fabricant dispose d’un design control complet, documenté et traçable.
• Les risques liés à l’usage réel ont été identifiés en amont, évitant des modifications tardives.
• L’évaluation formative a permis de corriger des points critiques avant la phase d’industrialisation.
• L’approche intégrée a réduit les itérations entre design, qualité, usage et réglementation.
• Le dispositif est désormais prêt pour la phase de vérification et pour la future sommative.
• La base documentaire fournit des garanties solides pour les dossiers CE et FDA.
Enseignements pour les fabricants
• Intégrer la 62366-1 dès la phase de conception permet de réduire les probabilités d'échec en évaluation sommative.
• Les exigences utilisateurs doivent être rédigées tôt et liées à des critères de test objectifs.
• Lier systématiquement risques produit et risques d’usage améliore la robustesse globale du design.
• La formative, lorsqu’elle est bien préparée, permet d’économiser du temps et de sécuriser le développement.
• La cohérence documentaire (DIR, RMF, UEF) est un facteur clé d’acceptation réglementaire.
Conclusion
Ce projet illustre l’impact d’une approche unifiée regroupant réglementation, design control, gestion des risques et facteurs humains. En structurant méthodiquement les exigences, l’analyse des risques et les activités usability, le fabricant a pu faire évoluer un prototype prometteur vers un dispositif maîtrisé, conforme et industrialisable.
Après plusieurs collaborations similaires, CSDmed et Usarea ont formalisé un partenariat pour offrir aux fabricants une continuité complète entre stratégie réglementaire, design control, maîtrise des risques et aptitude à l’utilisation.
Nous sommes disponibles pour échanger sur vos projets et vous aider à structurer un développement solide, efficace et conforme aux attentes CE et FDA.

Amandine Broussier
Spécialiste aptitude à l'utilisation chez Usarea